oleh Amrulloh
Teori Asam Basa Lewis
Asam adalah spesi yang bertindak sebagai penerima pasangan elektron
Basa adalah spesi yang bertindak sebagai donor pasangan elektron
H+ + H2O → H3O+
H+ + NH3 → NH4+
Struktur lewisnya:
Definisi dari lewis tidak bertentangan dengan teori asam basa bronsted Lowry, karena proton dapat dipandang sebagai penerima pasangan elektron. Spesi yang menerima proton dapat dipandang sebagai donor pasangan elektron.
Adapun keunggulan teori asam basa lewis adalah sbb:
1. Definisi lewis mencakup konsep-konsep basa yang tidak melibatkan tranfer proton
2. Dapat menjelaskan zat-zattertentu sebagai asam yang tidak mengandung hidrogen, tetapi berfungsi seperti asam
Contoh:
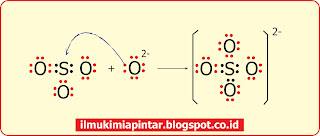
SO3 + O2- → SO42-
Struktur lewisnya:

Out Of Topic Show Konversi KodeHide Konversi Kode Show EmoticonHide Emoticon